SEKVENEERIMINE
DNA sekveneerimine e. järjendamine tähendab protsessi, mille käigus selgitatakse DNA nukleotiidne järjestus.
Meetodi looja oli 1977.aastal Frederick Sanger (üks vähestest kahekordsetest Nobeli preemia laureaatidest) ja protsessi põhimõte seisneb DNA ahela sünteesi peatamises "märgitud" (algusaegadel radioaktiivse märgisega, hiljem fluorokroomidega) dideoksünukleotiididega (ddNTP). VAATA.
(Korrektsuse huvides tuleb mainida, et enam-vähem samaaegselt loodi ka teine sekveneerimismeetod - Maxam-Gilberti e. keemiline meetod, mis erinevalt Sangeri omast, ei pidanud ajaproovile nii pikalt vastu.)
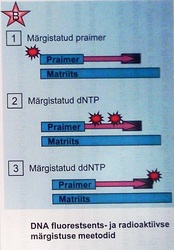
Piisava koguse algmaterjali ja reaktsioonikemikaalide korral toimub süntees samaaegselt paljudelt DNA molekulidelt ja reaktsioonianumas tekib igas pikkuses fragmente, mille süntees katkeb dideoksünukleotiidi ahelasse lülitumisega (Joon.13 A, B).
Kui saadud fragmentide segu geelelektroforeesil (PAGE) pikkuse järgi lahutada, siis selgub uuritud DNA nukleotiidide järjestus. Tänapäeval on see meetod tuntud kui Sangeri meetod, seda kasutades on 2001. aastal järjendatud ka inimese genoom.
(Korrektsuse huvides tuleb mainida, et enam-vähem samaaegselt loodi ka teine sekveneerimismeetod - Maxam-Gilberti e. keemiline meetod, mis erinevalt Sangeri omast, ei pidanud ajaproovile nii pikalt vastu.)
Piisava koguse algmaterjali ja reaktsioonikemikaalide korral toimub süntees samaaegselt paljudelt DNA molekulidelt ja reaktsioonianumas tekib igas pikkuses fragmente, mille süntees katkeb dideoksünukleotiidi ahelasse lülitumisega (Joon.13 A, B).
Kui saadud fragmentide segu geelelektroforeesil (PAGE) pikkuse järgi lahutada, siis selgub uuritud DNA nukleotiidide järjestus. Tänapäeval on see meetod tuntud kui Sangeri meetod, seda kasutades on 2001. aastal järjendatud ka inimese genoom.
|
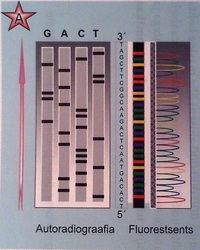
Laskumata aeganõudva geelivalmistamismetoodika ja reaktsioonide kokkusegamise üksikasjadesse, tasub siiski mainida, et "enne automatiseerimise aega" järgnes fragmentide geelil lahutamisele geelist röntgenpildi tegemine, seejärel saadud pildilt valguslaua kohal järjestuse veerimine ja nukleotiidide ühekaupa üleskirjutamine. Meetodite võrdlus lisatud kõrvalolevas galeriis. |
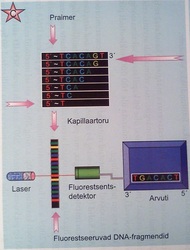
Joonis 13. A. Järjestatud DNA võrdlus radioaktiivsel ja fluorestsentsmärgistuse meetodil B. DNA märgistamise viisid C. Automaatsekveneerimine.
Allikas: Geneetika (2012) lk.326. |
Tänapäeval on kogu protsess automatiseeritud (Joon.13C). DNA-järjestus tuletatakse arvutiprogrammi abil fluoro-märgiste emissioonist ja fragmentide pikkusest. Pilt, mis saadakse automaatsekvenaatoriga avaneb siit.
Praegused tavakasutuse sekvenaatorid võimaldavad umbes 1000 nukleotiidi järjendamist ühest reaktsioonist.
Alates 1990.ndatest aastatest toimub sekveneerimisvaldkonnas tõeline "võidurelvastumine". Kõigi nende arendustega on kaasas käinud järjendamise kiiruse tõus ja selleks kuluva DNA-koguse vähenemine.
Viimastel aastatel on turule jõudnud ja korraga kasutusel erineva põhimõtte ja maksumusega uue põlvkonna sekveneerimisstrateegiaid (NGS) nagu näiteks Illumina HiSeq ja MiSeq, Roche 454, Life Technologies Ion Proton/Torrent ja SOLiD. NGSi võimalus (Illumina platvorm) on olemas ka Tartu Ülikoolis.
Sekveneerimise lihtsustumisega seoses suruvad üksiknukleotiidsed polümorfismid e. SNPd e. snipid kordusjärjestuste kasutamist kõrvale. Inimese kohta on teada, et SNPde sagedus kromosoomiti on erinev, samuti on (geograafiliselt) erinev see, mitu SNPd mingi arvu aluspaaride kohta esineb. Teiste organismide SNPde jaotuse ja sageduse kohta on andmeid palju vähem.
Andmemahu suurenemine seab suuri nõudmisi toorjärjestuste töötlemisele ja kokkupanemisele, eriti keeruline ja lahendamata on kordusjärjestuste paigutamine genoomides.
Iga uus järjendatud genoom lihtsustab järgmiste, sellele lähedaste, liikide genoomide järjendamist.
Positiivse "kõrvalsaadusena" on juba langenud ja langeb veelgi sekveneerimise hind aluspaari kohta. Sellest tulenevalt on genoomiinfo aina kättesaadavam ka sellistes valdkondades, kus tegeletakse nn. mitte-mudelorganismidega, nagu näiteks ka ökoloogia ja looduskaitse.
Alates 1990.ndatest aastatest toimub sekveneerimisvaldkonnas tõeline "võidurelvastumine". Kõigi nende arendustega on kaasas käinud järjendamise kiiruse tõus ja selleks kuluva DNA-koguse vähenemine.
Viimastel aastatel on turule jõudnud ja korraga kasutusel erineva põhimõtte ja maksumusega uue põlvkonna sekveneerimisstrateegiaid (NGS) nagu näiteks Illumina HiSeq ja MiSeq, Roche 454, Life Technologies Ion Proton/Torrent ja SOLiD. NGSi võimalus (Illumina platvorm) on olemas ka Tartu Ülikoolis.
Sekveneerimise lihtsustumisega seoses suruvad üksiknukleotiidsed polümorfismid e. SNPd e. snipid kordusjärjestuste kasutamist kõrvale. Inimese kohta on teada, et SNPde sagedus kromosoomiti on erinev, samuti on (geograafiliselt) erinev see, mitu SNPd mingi arvu aluspaaride kohta esineb. Teiste organismide SNPde jaotuse ja sageduse kohta on andmeid palju vähem.
Andmemahu suurenemine seab suuri nõudmisi toorjärjestuste töötlemisele ja kokkupanemisele, eriti keeruline ja lahendamata on kordusjärjestuste paigutamine genoomides.
Iga uus järjendatud genoom lihtsustab järgmiste, sellele lähedaste, liikide genoomide järjendamist.
Positiivse "kõrvalsaadusena" on juba langenud ja langeb veelgi sekveneerimise hind aluspaari kohta. Sellest tulenevalt on genoomiinfo aina kättesaadavam ka sellistes valdkondades, kus tegeletakse nn. mitte-mudelorganismidega, nagu näiteks ka ökoloogia ja looduskaitse.